Кавернозная гемангиома ректосигмоидного отдела толстой кишки больших размеров: клиническое наблюдение
Санников О. Р. 1, врач эндоскопист, к. м. н.
Фалалеев В. Л. 1, зав. отделением диагностики
Морозов С. Л. 2, врач патологоанатом
1 ФБУЗ МСЧ № 41 ФМБА России
2 МУЗ ЦРБ
г. Глазов
Гемангиомы и сосудистые мальформации желудочно-кишечного тракта относятся к редко встречающимся находкам, которые являются причиной как явных, так и скрытых кровотечений, представляющие собой доброкачественные сосудистые образования. Они могут встречаться в любом отделе желудочно-кишечного тракта, как в виде локальных (ограниченных) так и диффузных форм, одиночных (солидных) и множественных дефектов. Наиболее частой локализацией является тонкая кишка, где гемангиомы и сосудистые мальформации составляют до 10 % от всех неоплазий поражений данного отдела [1]. Толстая кишка поражается несколько реже, при этом ректосигмоидный отдел является самой частой локализацией данного вида образований [4]. Может иметь место сочетанное поражение с вовлечением печени, поджелудочной железы, желчного пузыря, кожи [2], гемангиомы больших размеров могут инфильтрировать матку, предстательную железу [8]; описаны варианты диффузного поражения практически всех отделов желудочно-кишечного тракта [3], а, также, случаи кишечной непроходимости, вызванные гигантскими гемангиомами толстой кишки [5].
Принципиальное отличие сосудистых мальформаций от гемангиом заключается в превалировании у последних стромального компонента над сосудистым, при динамическом наблюдении рост гемангиомы определяется стромой; в случае венозной мальформации объем поражения увеличивается за счет расширения сосудов [6,7]. Также, важным условием является отсутствие выраженного кровотока в кавернах гемангиом, в то время как в венозных мальформациях кровоток сохранен. Смешение этих двух понятий встречаемое в литературе, очевидно, связано с относительно недавним внедрением в клиническую практику метода эндосонографии, позволяющего дифференцировать вышеуказанные признаки этих сосудистых аномалий.
Впервые описание гемангиомы желудочно-кишечного тракта было дано в 1839 г. Phillips [5]. В классификации кишечных гемангиом выделяют следующие типы: капиллярный, кавернозный, который подразделяется на подтипы: локализованный (полипоидный или неполипоидный) и диффузно-инфильтративный (или экспасивный), а также, смешанный тип и гемангиоматоз [1]. 80 % ректальных гемангиом относятся к кавернозному типу. В целом, гемангиомы и сосудистые мальформации встречаются чаще у молодых женщин, чем у мужчин (соотношение 1:2.5), однако, в случае поражения толстой кишки, частота их обнаружения у представителей обоих полов примерно одинаковая [3].
Наиболее частым клиническим проявлением гемангиом толстой кишки является рецидивирующее ректальное кровотечение (более 75 % случаев); последнее может быть скрытым или массивным, нередко возникать еще в самом раннем возрасте, симулируя такие заболевания как внутренний геморрой, воспалительные заболевания толстой кишки (НЯК, болезнь Крона), карциному и ряд других, что может приводить к ошибочным заключениям и неправильному диагнозу [9]. Jeffery с соавт. [12] приводят данные, когда в 80 % случаев пациенты были подвергнуты, по крайней мере, одному необоснованному хирургическому вмешательству из-за ошибочного диагноза до того момента, когда факт наличия гемангиомы был достоверно подтвержден. В тех случаях, когда образование достигает больших размеров, могут возникать диарея, абдоминальные схваткообразные боли и кишечная непроходимость [10, 11]. Все вышеуказанное регламентирует строгий и ответственный подход к диагностическим мероприятиям, среди которых эндоскопический метод является наиболее оптимальным [6,13]. Биопсия сопряжена с высоким риском кровотечения, что может повлечь за собой необходимость экстренного хирургического вмешательства, однако, в ряде случаев она необходима для проведения дифференциального диагноза с некоторыми формами карцином и полиповидных образований [3]. Дифференциальный диагноз с венозными мальформациями проводится с помощью эндосонографии [14]. Мезентериальная ангиография используется для подтверждения диагноза и полезна для исключения “случайных” гемангиом в других отделах ЖКТ [3]. Неинвазивным исследованием, преследующим те же цели, является сонография. Дополнительную информацию о протяженности участка поражения, степени утолщения кишечной стенки, вовлеченности в процесс тазовой брюшины, количестве сосудистых образований может дать компьютерная томография [15]; высокая степень детализации слоев кишечной стенки и ее поверхности может быть достигнута использованием МРТ [16]. Специфичность рентгенологических признаков невысока [17].
Лечение зависит от объема (распространенности) поражения, клинических проявлений, наличия осложнений. Интермиттирующие кровотечения и анемия вынуждают прибегать к хирургическому вмешательству, которое является ведущим методом лечения таких больных. Выполняют резекцию пораженного участка кишки с формированием колоанального анастомоза [18]. В случае локализованных форм гемангиом возможны малоинвазивные методы воздействия, такие как инъекционная склерозирующая терапия, лазеротерапия, криотерапия, артериальная эмболизация, электрокоагуляция.
Приводим собственное клиническое наблюдение случая гемангиомы ректосигмоидного отдела толстой кишки больших размеров.
Пациентка Е. 1981 г. р. была направлена в эндоскопический кабинет нашего ЛПУ для проведения диагностической колоноскопии с жалобами на выделение неизмененной крови (гематохезис) во время акта дефекации. С 11 лет периодически беспокоят ректальные кровотечения. Имеет склонность к запорам. В 1998 г. при обследовании в проктологическом отделении I РКБ г. Ижевска был диагностирован “неспецифический язвенный колит”. Проходит курсы лечения сульфасалазином, прием препарата нерегулярный, без значимого эффекта. В ОАК Hb 90 г/л. Обследуется в МСЧ 41 впервые.
Во время выполнения колоноскопии проведен осмотр до уровня купола слепой кишки. В прямой кишке (нижняя граница, ориентировочно — зубчатая линия анального канала, верхняя граница — ректосигмоидный отдел, ~20 см от ануса) слизистая имеет необычный пестрый вид: участки белесовато-синюшного оттенка перемежаются с локусами в виде красных пятен неправильной формы и различной величины, как в виде скоплений, сливающихся друг с другом, так и отдельных “точечных” элементов, напоминающих интрамукозные петехии; здесь же визуализируются структуры, напоминающие сосудистую венозную ткань с варикозными изменениями, в виде конгломератов эластической консистенции; в среднеампулярном отделе прямой кишки просвет незначительно сужен за счет венозных вариксов, поверхность неравномерно бугристая; площадь поражения возрастает в дистальном направлении, захватывая в средне- и нижнеампулярном отделах кишки весь орган, в надампулярном — полуокружность органа (фото 2–7). Сосудистый рисунок в зоне поражения не прослеживается, зона демаркации находится в S‑romanum. Здесь же, располагаясь в непосредственной близости от сосудистых изменений — одиночное небольших размеров полиповидное образование “просовидной” формы (0.8х0.4х0.3 см) с неизмененной поверхностью (фото 1), биопсия его не проводилась ввиду потенциальной опасности кровотечения. Слизистая оболочка других, проксимально расположенных отделов толстой к‑ки розовая, сосудистый рисунок обычный, патологических изменений на ней не выявлено. При проведении аноскопии внутренние геморроидальные узлы располагаются в “типичных” местах, имеют синюшный оттенок с усиленным компонентом капиллярного рисунка, диаметр до 1.0 см, пролабируют в просвет аноскопа при натуживании. Начиная от уровня зубчатой линии и проксимальнее ее — вышеописанные изменения (фото 8,9).
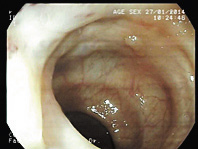








Заключение:
Гигантская кавернозная гемангиома ректосигмоидного отдела толстой кишки? Венозная мальформация? Хр. внутренний геморрой I ст.
Эндоскопическая картина, описанная выше, не соответствовала проявлениям, характерным для воспалительных заболеваний кишечника (НЯК, болезнь Крона, недифференцируемый колит). Эндометриоз кишечника также был исключен из за отсутствия характерных визуальных признаков несмотря на сложность эндоскопической диагностики (индурация и утолщение кишечной стенки, полиповидные, расположенные по окружности просвета стенотические зоны, нечётко отграниченные подслизистые опухоли, болезненность при проведении тубуса через пораженный сегмент и др.). Несмотря на то, что эндометриоз не всегда даёт симптоматику, больные страдают, как правило, во время месячных, обусловливающих развитие мучительных проявлений. Помимо дисменореи, встречаются спастические боли в области таза, диспареуния, тенезмы и болезненные дефекации. В сочетании с месячными может возникать кишечное кровотечение. Вышеперечисленные признаки у нашей пациентки отсутствовали.
Дополнительно было выполнено ультразвуковое сканирование стенки прямой кишки ректальным датчиком с частотой 5 Мгц и углом сканирования 180 градусов в режиме “ангиология” (small vessels). При исследовании в серой шкале отмечается утолщение подслизистого слоя до 0.9–1 см в пределах которого визуализируются гипоэхогенные образования неправильной формы, размерами (в поперечнике) от 2 до 10 мм (рис. 1). При цветовом дуплексном картировании определяется хороший кровоток имеющий венозный и артериальный компоненты в мышечном и подслизистом слоях прямой кишки, признаков аневризм, мальформаций не выявлено. В области вышеописанных гипоэхогенных образований наличия кровотока по ЦДК и допплер-ЭХО-КГ не выявлено. Эхографическая картина не противоречит диагнозу «кавернозная гемангиома» (“рутинное” УЗИ с использованием ректального датчика уступает в точности эндоскопической сонографии и не позволяет достоверно оценить соотношение стромального и сосудистого компонентов в структуре измененной ткани, тем не менее, с помощью данного исследования было подтверждено отсутствие кровотока в кавернозных структурах, что является важным дифференциальным критерием в пользу гемангиомы).
Необходимо отметить тот факт, что больная в течение многих лет получала лечение от другого заболевания. Неправильная интерпретация полученных данных может быть обусловлена нетипичностью визуальных проявлений патологического процесса, в т. ч. и редко встречающихся находок, техническими ограничениями (недостаточная подготовка пациента), наконец, формальным отношением исследователя к процедуре, стремлением уложить обнаруженные изменения в “прокрустово ложе” наиболее часто встречающихся нозологий. Это подчеркивает важность соблюдения стандартов диагностического процесса на всех этапах; при этом наибольшая составляющая принадлежит тщательной визуальной оценке выявленных изменений во время эндоскопического исследования, являющегося одним из ведущих методов диагностики данных аномалий.
Список литературы:
1. Stephen Y. GI-Associated Hemangiomas and Vascular Malformations. Clinics in colon and rectal surgery. 09/2011; 24 (3):193–200.
2. Lyon DT, Manita AG. Large-bowel hemangiomas. Dis Colon Rectum 1984; 27: 404–414.
3. Erkan G., Alagozlu H., Memis L, Tuncer C. Rapidly growing giant solitary cavernous hemangioma in a patient with ulcerative colitis//Turk J Gastroenterol 2008; 19 (4):271–275.
4. Angela D. Levy, Robert M Abbott, Charles A Rohrmann, Jr. Gastrointestinal hemangiomas: Imaging findings with pathologic correlation in pediatric and adult patients. AJR Am О Roengenol 2001; 177:1073–1081.
5. Demirbas T, Guler N, Caliscan C, et al. Mechanical bowel obstruction due to colonic hemangioma: report of a case. Turk J Gastroenterol 2006; 17:305–7.
6. Fenandez-Pineda I. Vascular tumors and malformations of the colon//World О Gastroenterol 2009 November 7; 15 (41): 5242–5243.
7. Frieden I, Enjolras O, Esterly N. Vascular birthmarks and other abnormalities of blood vessels and lymphatics. In: Shachcner LA, Hansen RC, editors. Pediatric dermatology. 3rd ed. Saint Louis.MO: Mosby, 2003: 833–862.
8. Wai-Yip, Chin-Chu Wu, Liang-Kuang Chen, Chen-Tau Su. Giant Hemangioma of the rectum: a case report//Chin J Radiol 2005; 30:133–137.
9. Stening SG, Heptinstall DP. Diffuse cavernous hemangioma of the rectum and sigmoid colon. Br J Surg 1970;57: 186–9.
10. Gentry RW, Dockerty MB, Clagett OT. Vascular malformations and vascular tumours of the gastrointestinal tract. Int Abstr Surg 1949; 88:281–323.
11. Allred HW, Spencer RJ. Hemangiomas of the colon, rectum and anus. Mayo Clin Proc 1974; 49:739–41.
12. Jeffery PJ, Hawley PR, Parks AG. Colo-anal sleeve anastomosis in the treatment of diffuse cavernous hemangioma involving the rectum. Br J Surg 1976;63:678–82.
13. Bugra D, Bulut T, Yamaner S, et al. Soft-tissue images. Diffuse cavernous rectal hemangioma. Can J Surg 2002;45:365–6.
14. Солоницын Е. Г. Гигантская гемангиома ректосигмоидного отдела толстой кишки: демонстрация клинического случая//Клиническая эндоскопия 2011; 3 (29): 18–21.
15. Sharma S, Gandhi D, Thulkar S, Dwivedi DN. Role of computed tomography in diagnosis of diffuse cavernous hemangioma of the rectum. Am J Gastroenterol 1999;94:1986–7.
16. Yorozuya K, Watanabe M, Hasegawa H, et al. Diffuse cavernous hemangioma of the rectum: report of a case. Surg Today 2003;33:309–11.
17. Bell GA, McKenzie AD, Emmons H. Diffuse cavernous hemangioma of the rectum: report of a case and review of the literature. Dis Colon Rectum 1972;15:377–82.
18. Ruchit Sood, Deepika Chilkunda, John Brittenden, Deven Vani Chronic Haematochezia Caused by Diffuse Cavernous Haemangioma of the Rectum//Journal of gastrointestinal and liver diseases: JGLD 03/2013; 22 (1):12–15.


