Этапное эндоскопическое лечение лучевого проктосигмоидита, осложнённого рецидивирующим кровотечением
Иванова Е. В., д. м. н.,
ст. н. сотр. НИЛ хирургической гастроэнтерологии и эндоскопии; врач-эндоскопист, ведущий специалист по эндоскопии Медицинского реабилитационного центра «Клиника К+31»
Федоров Е. Д.,
профессор, д. м. н., гл. н. сотр. НИЛ хирургической гастроэнтерологии и эндоскопии, клин. зав. отделением оперативной эндоскопии ГКБ № 31
Тихомирова Е. В.,
ординатор кафедры госпитальной хирургии № 2 и НИЛ хирургической гастроэнтерологии и эндоскопии
ГБОУ ВПО «РНИМУ им. Н. И. Пирогова» Минздрава России
г. Москва
Хронический лучевой проктосигмоидит является одним из частых осложнений лучевой терапии, проводимой по поводу онкологических заболеваний малого таза, и составляет, согласно литературным данным, от 2 до 20 % [3,4]. Как правило, время возникновения хронического постлучевого колита варьируется от 8 до 12 месяцев от момента окончания лучевой терапии [1].
Терапией «первой линии» считаются препараты 5‑аминосалициловой кислоты в сочетании с глюкокортикостероидами. Применение сукральфата способствует улучшению состояния у 75 % пациентов. Однако в случае, если консервативное лечение оказывается неэффективным, рекомендуется эндоскопическое лечение, включающее аргоно-плазменную коагуляцию, применение формалина или эндоскопическую каутеризацию [2]. Применение формалина безопасно, однако он не может использоваться при обширных поражениях [2]. Преимущество аргоно-плазменной коагуляции состоит в небольшой глубине проникновения энергии в ткани (от 0,5 до 3 мм), что позволяет коагулировать поверхностно расположенные сосуды кишки [2, 4]. Yasushi Sato и соавт. показали, что неоднократное использование аргоно-плазменной коагуляции с недельным интервалом при тяжелом поражении слизистой оболочки толстой кишки является эффективным и безопасным методом лечения лучевого колита [4].
Представленное клиническое наблюдение иллюстрирует эффективность эндоскопического лечения лучевого проктосигмоидита, осложненного рецидивными кровотечениями.
Больная Ш., 76 лет, 15.04.2012 г. была госпитализирована в Медицинский реабилитационный центр «Клиника+31» г. Москвы с жалобами на примесь крови в стуле, выраженную слабость и одышку при минимальной физической нагрузке на протяжении последних 7 месяцев.
Из анамнеза известно, что с июля по сентябрь 2010 года пациентке проводилась лучевая терапия (общей дозой 40 Грей) по поводу рака шейки матки T2bNxM0 стадии. В августе 2011 года пациентка была экстренно госпитализирована в одну из клиник г. Москвы с жалобами на учащение стула до 3 раз в сутки, примесь крови в кале и выраженную слабость. Клинической картине сопутствовала анемия тяжелой степени (гемоглобин — 64 г/л, эритроциты — 2,28х10¹²/л, гематокрит — 24,1 %). При колоноскопии было выявлено большое количество сгустков и свежей крови в просвете толстой кишки, затрудняющих тщательный осмотр, а также множественные ангиоэктазии прямой кишки и дистальной части сигмовидной ободочной кишки, локализующиеся по всем стенкам, тенденцией к слиянию, и с протяженностью распространения до 35 см от ануса. Таким образом, был диагностирован лучевой проктосигмоидит тяжелого течения и рекомендовано консервативное лечение. С августа 2011 года по март 2012 года пациентка принимала препараты 5‑аминосалициловой кислоты, перорально 500 мг х 2 раза в день и в виде клизм (однократно, на ночь), глюкокортикостероиды по 1 капсуле (3 мг) 3 раза в день, гемостатические препараты: дицинон по 2 таблетки 3 раза в день, викасол по 2 таблетки (по 15 мг) 1 раз в день, и препарат железа: тотема (100 мг) по 2 ампулы в сутки. Однако самочувствие пациентки оставалось прежним, уровень гемоглобина составлял 94 г/л.
При колоноскопии, проведенной 28.03.2012, были выявлены множественные ангиоэктазии и кровь в прямой кишке и дистальной части сигмовидной кишки, в связи с чем пациентке было рекомендовано эндоскопическое лечение с применением аргоно-плазменной коагуляции (АПК). С целью выполнения эндоскопического лечения, пациентка обратилась к нам в клинику 16.04.2012 г. При колоноскопии в прямой кишке имелся крупный сгусток крови, отмечалась контактная кровоточивость ранее описанных множественных ангиоэктазий прямой кишки и дистальной части сигмовидной ободочной кишки, на протяжении 35 см от ануса (Рис. 1, 2).


Рис.1, 2. Эндофотография. Множественные ангиоэктазии сигмовидной ободочной кишки
После отмывания кишки от крови была выполнена АПК восьми кровоточащих ангиоэктазий (Рис. 3–5), однако в связи с возникновением выраженного болевого синдрома, с учетом длительности вмешательства, было решено разбить его на несколько этапов.
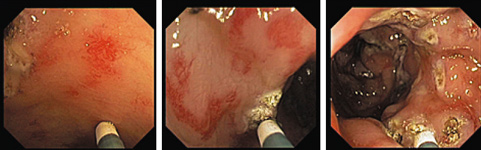
Рис.3, 4, 5. Эндофотография. Аргоно-плазменная коагуляция ангиоэктазий сигмовидной и прямой кишки
Через 2 дня после первого этапа пациентке был успешно выполнен второй этап аргоно-плазменной коагуляции ангиоэктазий, образующих точечные и сливные поля в сигмовидной и прямой кишке. Послеоперационный период протекал благоприятно, и через 6 дней она была выписана из стационара в удовлетворительном состоянии: примеси крови в стуле не было, оставались только жалобы на одышку при физической нагрузке. Пациентке была рекомендована повторная госпитализация в стационар в плановом порядке для контрольного осмотра и проведения очередного этапа аргоно-плазменной коагуляции.
Через месяц, 30.05.2012 года, пациентка вновь была госпитализирована в клинику с жалобами на примесь крови в кале и слабость, которым сопутствовала анемия легкой степени тяжести (гемоглобин — 104 г/л, эритроциты — 3,51х10¹²/л, гематокрит — 33,2 %). При колоноскопии (31.05.2012): в прямой кишке был выявлен сгусток крови, после отмывания выявлены ангиоэктазии в прямой и сигмовидной кишке с подтеканием крови, а также изъязвления слизистой оболочки, образовавшиеся в результате предыдущих этапов АПК (Рис. 6). С целью остановки кровотечения в подслизистой слой в места наиболее выраженных ангиоэктазий было введено до 10 мл физиологического раствора с адреналином, что вызвало побеление слизистой, остановку кровотечения и более четкую визуализацию сосудистых структур (Рис. 7). После этого поэтапно, в дистальном направлении, с нижней трети сигмовидной кишки в направлении ануса, была выполнена аргоно-плазменная коагуляция ангиоэктазий; при наблюдении после вмешательства данных за кровотечение не было (Рис. 8–9). Послеоперационный период протекал гладко, пациентка была выписана из стационара через 5 дней в удовлетворительном состоянии. Стул нормализовался, примесь крови в кале исчезла, симптомы анемии уменьшились (кожа обычной окраски, цианоз губ уменьшился, гемоглобин 114 г/л).

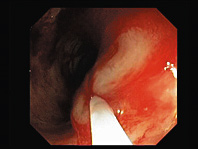


Рис.8-9. Эндофотография. Аргоно-плазменная коагуляция ангиоэктазий сигмовидной и прямой кишки после введения физиологического раствора с адреналином
Через год после третьего этапа аргоно-плазменной коагуляции пациентка отмечала улучшение самочувствия, отсутствие примеси крови в кале и слабости, а при проведении контрольного общего анализа крови было выявлено восстановление уровня гемоглобина до 142 г/л (эритроциты — 4,9х10¹²/л, гематокрит — 41 %).
Таким образом, представленный клинический случай демонстрирует эффективность применения эндоскопической аргоно-плазменной коагуляции в лечении лучевого проктосигмоидита. Применение раствора с добавлением адреналина до выполнения аргоно-плазменной коагуляции помогает уменьшить кровоточивость сосудистых структур и обеспечивает „чистое операционное поле” для прицельного и более эффективного воздействия. Для достижения качественного результата лечения лучевого проктосигмоидита требуется поэтапное лечение.
Список литературы:
1. A. Denton, A. Forbes, J. Andreyev, and E. J. Maher. Non surgical interventions for late radiation proctitis in patients who have received radical radiotherapy to the pelvis. Cochrane Database of Systematic Reviews. — 2002. — № 1. — Article ID CD003455.
2. Do N. L., Nagle D, Povlin V. Radiation Proctitis: Current Strategies in Management. — Gastroenterology Research and Practice. — 2011. — Article ID 917941.
3. P. P. Tagkalidis P. P., J. J. Tjandra J. J. Chronic radiation proctitis. — ANZ Journal of Surgery. — 2001. — Vol. 71. — №.4. — P. 230–237.
4. Sato Y. et al. Argon plasma coagulation treatment of hemorrhagic radiation proctopathy: the optimal settings for application and long-term outcome. Gastrointestinal Endoscopy. — 2011. — Vol. 73. — No.3 — p.543–549.

